
2025年4月11日,我院刘艳明教授团队在Nature Communications期刊发表题为“Insights into lattice oxygen and strains of oxide-derived copper for ammonia electrosynthesis from nitrate”的研究论文,团队成员吴钦岳为论文第一作者,刘艳明为论文通讯作者。
论文报道了含有残余晶格氧和晶格应变的氧化物衍生铜纳米片阵列(OD-Cu NSs),以促进通过eNO3RR合成NH3的性能。在中性溶液、10-140 mM NO3-和50-1500 mA·cm−2条件下,NH3的法拉第效率为88.7-99.7%,NH3产率最高为6.20 mmol·h−1·cm−2。实验和理论结果表明,晶格氧调节了OD-Cu NSs的电子结构,促进了*NO2的转化,而晶格应变促进了水解离生成*H,从而使其具有良好的NH3合成性能。通过eNO3RR所得氨化合物高回收率证明了OD-Cu NSs的适用性。
研究人员设计了含有残余晶格氧和晶格应变的氧化物衍生铜纳米片阵列(OD-Cu NSs)来调节eNO3RR过程中*NO2的吸附强度和*H的供应。实验和密度泛函理论DFT计算结果表明,残余的晶格氧调节了Cu表面的电子状态,减少了对*NO2的吸附并促进了其转化。晶格拉伸应变增强了水解离产生的*H供应。结果表明,在中性溶液和50-1500 mA·cm−2条件下,OD-Cu NSs合成NH3的法拉第效率(FEs)高达88.7-99.7%,超过了近期报道的催化剂。通过NO3-还原有效回收NH3和NH4Cl,证明了该催化剂的应用潜力。
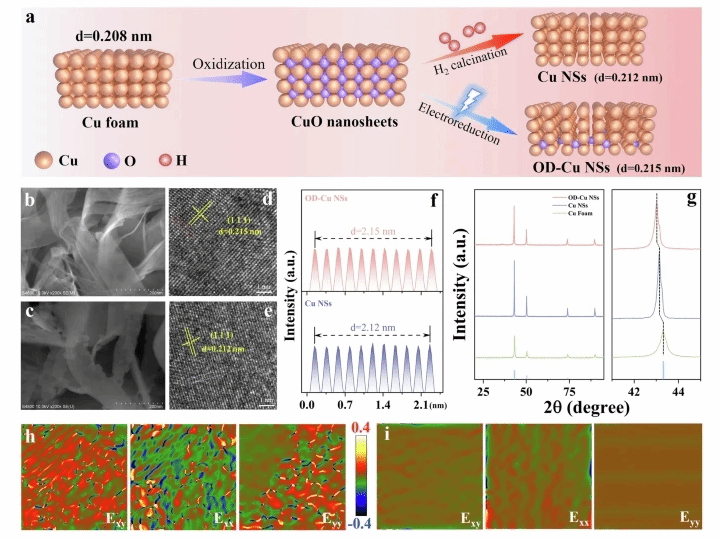
图1:Cu NSs和OD-Cu NSs合成示意图。a Cu NSs和OD-Cu NSs合成示意图。b-e 分别为OD-Cu NSs (b, d)和Cu NSs (c, e)的 SEM图像和HRTEM图像。f Cu NSs和OD-Cu NSs的晶格间距。g XRD图谱。h, i 基于HRTEM图像绘制的OD-Cu NSs (h)和Cu NSs (i)在Exy, Exx和Eyy处的应变场图。
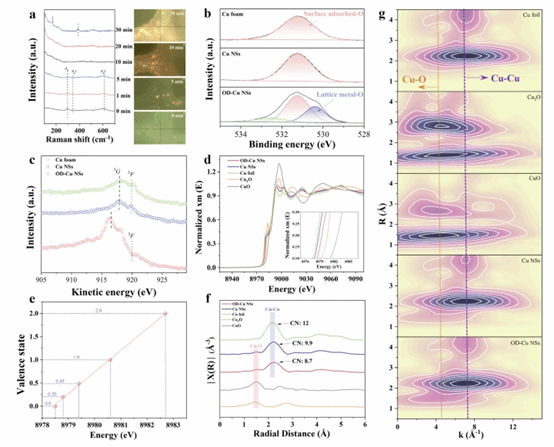
图2:结构表征。a 在−0.87 V下OD-Cu NSs表面的operando拉曼光谱(左图)和时间分辨光学显微镜图像(右图)。Cu泡沫、Cu NSs和OD-Cu NSs的b O 1s XPS光谱和(c) Cu L3M45M45俄歇光谱。d Cu K边XANES光谱。e 拟合的价态。Cu箔,Cu2O, CuO,Cu NSs和OD-Cu NSs的f 对应的k3加权FT-EXAFS光谱和(g) k3加权EXAFS数据的Morlet WT。
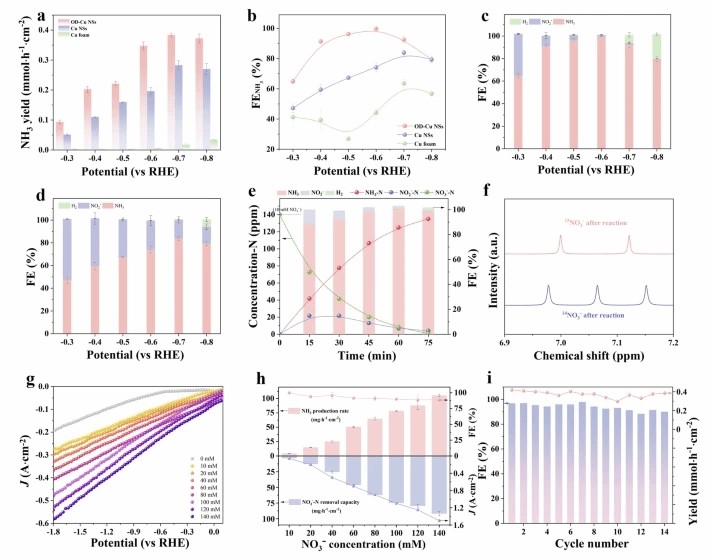
图3:eNO3RR的性能。使用Cu泡沫、Cu NSs和OD-Cu NSs催化10 mM NO3−还原时的a NH3产率和(b) 对应的FEs。c, d (c) OD-Cu NSs和(d)Cu NSs的产物分布。e 使用OD-Cu NSs催化10 mM NO3−还原时NO3−、NO2−和NH3浓度随时间的变化情况。f OD-Cu NSs催化15NO3−或14NO3−还原样品的1H NMR谱图。使用OD-Cu NSs催化10 ~ 140 mM NO3−还原时的g LSV曲线,和(h) 硝酸盐去除性能和NH3产率。i 在−0.6 V(Na2SO4电解质)下,10 mM NO3−还原连续14次循环时OD-Cu NSs的稳定性。误差条表示三个独立测量的标准差。所有的势都没有经过iR校正。
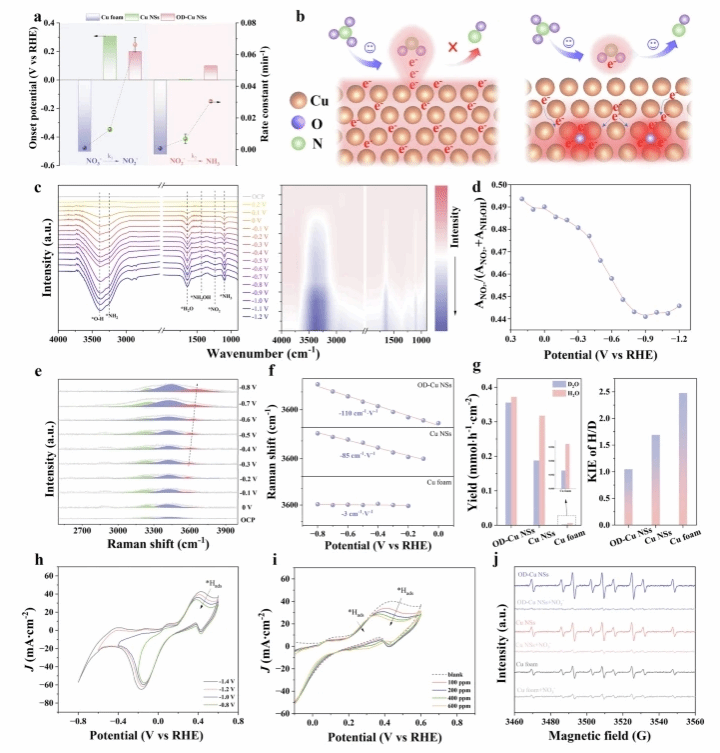
图4 *NO2转化和*H生成机理分析。a 在0.5 M Na2SO4 + 10 mM NO3−/NO2−条件下,OD-Cu NSs、Cu NSs和Cu泡沫上NO3−转化为NO2−的起始电位和反应常数(k1)和NO2−转化为NH3的起始电位和反应常数(k2)(误差条表示三次独立测量的标准差)。b 晶格氧引起的中间体吸附在Cu表面的示意图。c operando ATR-FTIR光谱和二维FTIR等高线图。不同电位下OD-Cu NSs上eNO3RR过程中不同界面水的d ANO2/ANO2 + ANH2OH和e 原位拉曼光谱。f 悬挂状态O-H的波数移位随电位变化情况。g 在−0.6 V下,以H2O和D2O为溶剂,eNO3RR的NH3产率和KIE值。(h) 在不同启动电位、Ar饱和0.5 M Na2SO4和(i) 不同NO3−浓度下OD-Cu NSs的循环伏安图。j −0.6 V下,添加和不添加硝酸盐时OD-Cu NSs、Cu NSs和Cu泡沫的*H信号EPR谱。所有的势都没有经过iR校正。
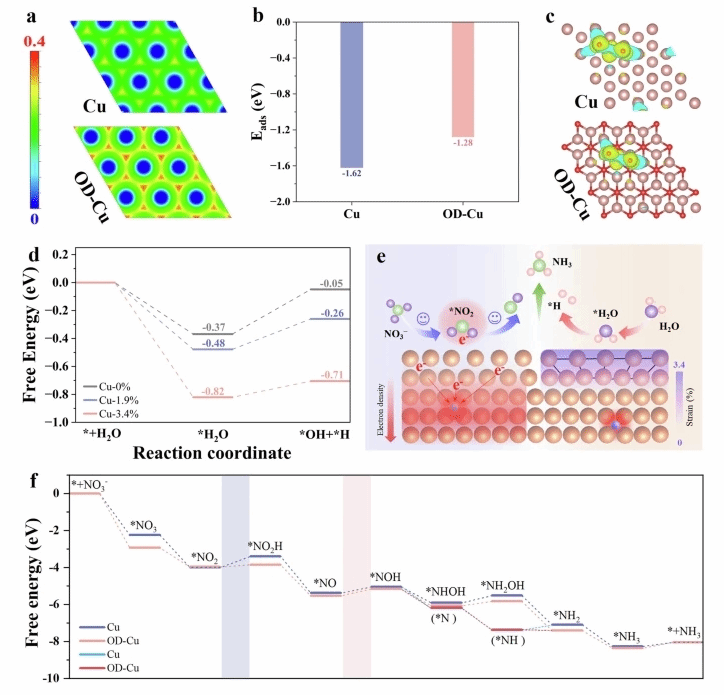
图5:DFT计算的反应机理。Cu和OD-Cu表面NO2-的a ELF 图和(b) 吸附能。c Cu和OD-Cu的吸附模型和电荷密度差(电子的积累和缺失用蓝色和黄色表示)。d 在Cu-0%、Cu-1.9%和Cu-3.4%表面上H2O解离生成*H的Gibbs自由能。e 晶格氧导致的电子调节和晶格应变导致的水解离促进eNO3RR的示意图。f 在Cu和OD-Cu表面eNO3RR的吉布斯自由能图。
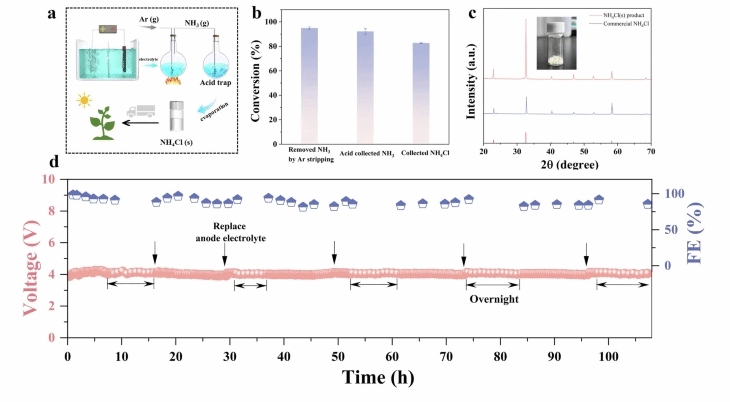
图6:氨回收率和稳定性。a 将硝酸盐转化为高纯度NH4Cl过程的示意图。b 在−1.1 A cm−2下还原100 mM NO3−合成NH3的转化效率(误差条表示三个独立测量的标准差)。c 合成NH4Cl产物的XRD图谱。d 使用MEA系统(30 mM NO3−,1.0 A, 4.0 cm2, Na2SO4电解质)的OD-Cu NSs上eNO3RR的长期稳定性。
总之,该研究用简单方法制备了具有残余晶格氧和晶格拉伸应变的OD-Cu NSs。OD-Cu NSs在10 mM NO3-和中性溶液中具有很高的eNO3RR活性和稳定性,FENH3接近100%。在NO3-浓度范围内(10-140 mM),在50-1500 mA·cm−2条件下,NH3的电合成效率很高,FENH3为88.7-99.7%,NH3产率最高为6.20 mmol·h-1·cm−2。它将80%以上100 mM的NO3-转化为高纯度NH4Cl。OD-Cu NSs具有优异的性能,是由于晶格应变导致的残余晶格氧和水解离导致的电子调节,并且加速了eNO3RR合成NH3的*NO2转化和*H供应。该研究拓宽了对电催化机理的理解,并将为在其他领域提高电催化性能开辟新的可能性。